30/01/2022
Las proteínas son las máquinas moleculares de la vida, y su capacidad para llevar a cabo funciones específicas, desde catalizar reacciones hasta transportar moléculas, depende fundamentalmente de su intrincada estructura tridimensional. Sin embargo, en ciertos procesos, como la producción de proteínas recombinantes en laboratorio, las proteínas pueden perder esta estructura vital, un fenómeno conocido como desnaturalización. La renaturación de proteínas es el arte y la ciencia de restaurar la forma nativa y funcional de una proteína desnaturalizada, un paso crítico para su aplicación en campos como la medicina, la investigación y la industria.

El objetivo principal de la renaturación es guiar las cadenas polipeptídicas desordenadas hacia su conformación tridimensional correcta. No obstante, este proceso no está exento de desafíos, siendo el más significativo la prevención de la agregación. Cuando una proteína se desnaturaliza, expone regiones hidrofóbicas que normalmente estarían ocultas en el interior de su estructura. Al intentar replegarse, estas regiones pueden interactuar con las de otras moléculas de proteína, llevando a la formación de agregados insolubles y no funcionales, en lugar de proteínas individuales y activas.
El Desafío Central: Prevenir la Agregación Proteica
El principal obstáculo en el replegamiento de proteínas es evitar la agregación a medida que la proteína inicialmente desnaturalizada pasa por estados intermedios parcialmente plegados. Esto ocurre cuando se elimina el agente desnaturalizante del búfer de solubilización. En estos estados intermedios, las proteínas son particularmente vulnerables a interacciones intermoleculares no deseadas, ya que sus superficies hidrofóbicas quedan expuestas al solvente. La clave para una renaturación exitosa reside en equilibrar las condiciones para permitir el plegamiento intramolecular mientras se minimiza la asociación intermolecular.
Clasificación General de los Métodos de Renaturación
Las diferentes metodologías para el replegamiento de proteínas se pueden clasificar ampliamente en dos categorías principales: enfoques basados en solución y enfoques basados en columna. Cada uno ofrece ventajas y desventajas, y la elección del método óptimo a menudo depende de las propiedades específicas de la proteína, la escala de producción y los recursos disponibles.
Métodos Basados en Solución
Los enfoques basados en solución se llevan a cabo en diversas configuraciones, dependiendo de cómo se elimina el desnaturalizante y cómo se añade la proteína a la solución de renaturación. Un factor clave en la elección de cualquier método es el efecto de la concentración del desnaturalizante, que controla las poblaciones relativas de los intermedios de plegamiento y sus tasas de interconversión y asociación intermolecular. A alta concentración de desnaturalizante, la proteína tiene una estructura muy flexible, los intermedios estarán más poblados y todas las formas de asociación intermolecular se debilitan. Reducir la concentración de desnaturalizante conduce al colapso y plegamiento de la proteína, pero también aumenta la asociación intermolecular, que a su vez depende de los tipos de intermedios que se forman. Los intermedios con mayores grados de desplegamiento y más grupos hidrofóbicos expuestos al solvente tienen mayores propensiones a la asociación. Encontrar la concentración óptima requiere hallar dónde la proteína puede interconvertir entre especies, pero también permanecer soluble.
1. Métodos de Dilución
La dilución de la proteína solubilizada directamente en el búfer de renaturación es el método más comúnmente utilizado para el replegamiento a pequeña escala de proteínas recombinantes. Es simple y directo. Sin embargo, el replegamiento de grandes cantidades de proteína recombinante mediante un método de dilución requiere un gran recipiente de replegamiento, una enorme cantidad de búfer y pasos de concentración adicionales después de la renaturación de la proteína, lo que aumenta el alto costo de producción de proteínas.
A escala de laboratorio, las alternativas a la dilución rápida son la dilución inversa, donde el búfer de replegamiento se añade en pasos secuenciales a la solución de proteína desnaturalizada, y la dilución por goteo (drip dilution), donde la solución de proteína desnaturalizada se añade al búfer de replegamiento de manera lenta y gradual. El equivalente a gran escala de la dilución por goteo es la dilución pulsada o por lote alimentado.

La dilución inversa no se utiliza comúnmente porque la concentración de proteína es más alta a una concentración moderada de desnaturalizante, lo que aumenta las posibilidades de agregación cuando la proteína pasa por la transición de replegamiento. En la dilución por goteo o pulsada, siempre que el tiempo de dilución característico sea más lento que la tasa de replegamiento, la proteína se repliega al estado nativo de modo que la concentración del intermedio de replegamiento se mantiene en una concentración mínima. Este método funciona siempre y cuando la proteína plegada nativamente no esté disponible para agregarse, pero se vuelve lento para proteínas con tasas de plegamiento lentas. Una preocupación clave para la dilución pulsada o por lotes es que se producen altas concentraciones locales de proteína inmediatamente después de añadir la solución de proteína desnaturalizada. Como tal, es necesario desarrollar varios métodos de mezcla para reactores por lotes para mantener los tiempos de mezcla menores que el tiempo de agregación característico y para mejorar los rendimientos.
2. Métodos Basados en Diálisis
El desnaturalizante se puede eliminar de manera gradual utilizando métodos basados en diálisis. Estos se pueden llevar a cabo en un procedimiento de un solo paso, donde la solución se dializa contra el búfer de renaturación final. Alternativamente, la concentración de desnaturalizante en el dializado se puede reducir en intervalos de pasos (diálisis de múltiples pasos) o en un gradiente continuo.
Las ventajas clave de los métodos de diálisis son que evitan las regiones locales de alta concentración de proteína, lo cual es problemático en los métodos de dilución, y hay más control sobre las tasas de replegamiento, de modo que la cantidad de proteína mal plegada se puede minimizar. Sin embargo, la competencia entre las tasas de agregación y replegamiento en función de la concentración de desnaturalizante varía entre las proteínas. Como tal, en algunos casos, la diálisis puede conducir a rendimientos reducidos cuando las tasas de agregación se mejoran en ciertas ventanas de concentración de desnaturalizante. Por el contrario, la diálisis es ideal cuando los intermedios de plegamiento son solubles en todas las concentraciones de desnaturalizante.
En la diálisis de múltiples pasos, la solución de proteína se deja equilibrar con concentraciones decrecientes de desnaturalizante de manera gradual. Este método se utiliza en algunos casos para proteínas que contienen enlaces disulfuro y algunas proteínas multidominio. Se requiere una concentración moderada de desnaturalizante para mantener suficiente flexibilidad de la proteína que permita la interconversión entre los enlaces disulfuro hasta que se forme la estructura correcta. Si la concentración de desnaturalizante es demasiado baja, existe una gran barrera de activación para cualquier reordenamiento conformacional que corrija los enlaces disulfuro formados incorrectamente. Además, el método se utiliza para proteínas que contienen múltiples dominios con diferentes estabilidades conformacionales. La equilibración a una concentración más alta de desnaturalizante puede usarse para equilibrar el dominio más estable, lo que generalmente conducirá a mayores rendimientos de replegamiento a la concentración más baja de desnaturalizante requerida para plegar el dominio menos estable.
Métodos Basados en Columna (Cromatográficos)
La otra alternativa para la renaturación es utilizar enfoques basados en cromatografía. Estos métodos ofrecen ventajas significativas al proporcionar un entorno controlado que puede mitigar la agregación.
1. Cromatografía de Exclusión por Tamaño (SEC)
El replegamiento se puede lograr utilizando cromatografía de exclusión por tamaño (SEC) para proporcionar un gradiente gradual en la concentración de desnaturalizante. La principal ventaja de este método es que la proteína también se fracciona por tamaño durante el paso, lo que puede ayudar a separar los agregados de las proteínas monoméricas correctamente plegadas.
2. Renaturación 'On-Column'
Alternativamente, en las técnicas de replegamiento 'on-column', el desnaturalizante se elimina mientras la proteína está adsorbida en la fase estacionaria de la columna. Se cree que este enfoque previene la agregación a través de efectos de volumen excluido y al separar las moléculas de proteína entre sí a medida que pasan por los estados intermedios propensos a la agregación. Se pueden utilizar varios modos de captura, incluyendo columnas de interacción hidrofóbica, resinas de intercambio iónico o ligandos de afinidad. Además, se pueden inmovilizar chaperonas de plegamiento en la fase estacionaria para mejorar los rendimientos de replegamiento.
Tabla Comparativa de Métodos de Renaturación
| Método | Principio Clave | Ventajas | Desventajas | Aplicaciones Típicas |
|---|---|---|---|---|
| Dilución Rápida | Reducción abrupta del desnaturalizante. | Simple, rápido para pequeña escala. | Agregación alta a concentraciones elevadas, grandes volúmenes para gran escala. | Renaturación de prueba, optimización inicial. |
| Dilución Lenta (Goteo/Pulsada) | Adición gradual de proteína a buffer. | Reduce agregación, control sobre intermedios. | Lenta, riesgo de concentraciones locales altas. | Proteínas con plegamiento lento. |
| Diálisis (Multi-paso) | Eliminación gradual y controlada del desnaturalizante. | Evita puntos calientes de concentración, control preciso de tasas. | Puede ser lenta, menor rendimiento si la agregación es alta en rangos específicos. | Proteínas con puentes disulfuro, multidominio. |
| Cromatografía de Exclusión por Tamaño (SEC) | Gradiente de desnaturalizante a través de la columna. | Fraccionamiento por tamaño, separación de agregados. | Requiere equipo cromatográfico, limitado por la capacidad de la columna. | Purificación y renaturación simultánea. |
| Renaturación 'On-Column' | Proteína adsorbida a fase estacionaria, eliminación de desnaturalizante. | Previene agregación por separación física, uso de chaperonas inmovilizadas. | Requiere optimización de la fase estacionaria, posible unión inespecífica. | Proteínas con alta tendencia a la agregación, producción a gran escala. |
Preguntas Frecuentes sobre la Renaturación de Proteínas
¿Qué es la renaturación de proteínas?
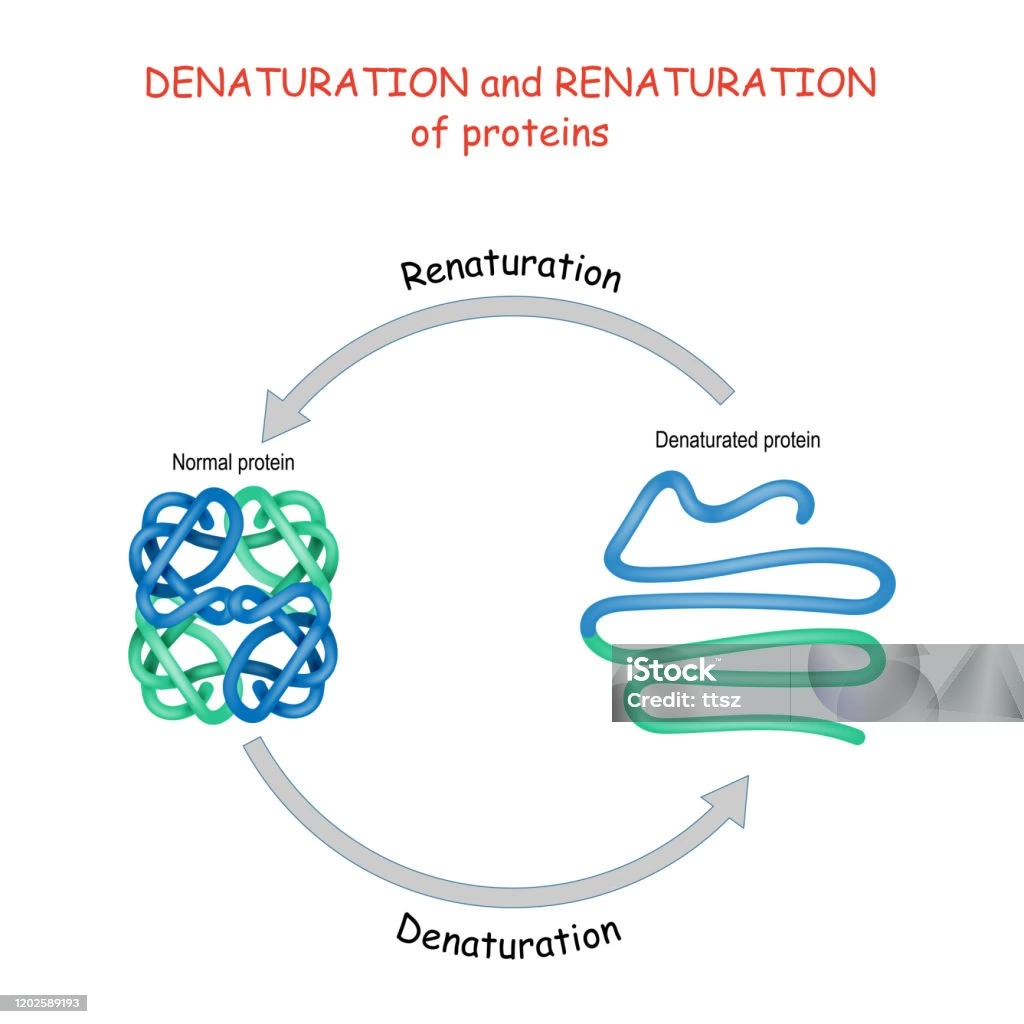
La renaturación de proteínas es el proceso mediante el cual una proteína desnaturalizada, es decir, que ha perdido su estructura tridimensional y, por ende, su función biológica, recupera su conformación nativa y funcional. Este proceso es fundamental en biotecnología para obtener proteínas activas a partir de cuerpos de inclusión o de proteínas producidas en condiciones de estrés.
¿Por qué es tan difícil lograr una renaturación eficiente?
El mayor desafío en la renaturación es evitar la agregación de las proteínas. Durante el proceso de eliminación del agente desnaturalizante, las proteínas pasan por estados intermedios en los que sus regiones hidrofóbicas, normalmente ocultas, quedan expuestas. Estas regiones pueden interactuar con las de otras moléculas de proteína, formando agregados insolubles en lugar de plegarse correctamente en su forma activa. Controlar estas interacciones es clave para el éxito.
¿Cuáles son las principales estrategias para renaturar proteínas?
Las estrategias se dividen principalmente en métodos basados en solución y métodos basados en columna. Los métodos en solución incluyen la dilución (rápida, inversa, por goteo/pulsada) y la diálisis. Los métodos basados en columna utilizan técnicas cromatográficas como la cromatografía de exclusión por tamaño (SEC) o la renaturación 'on-column', donde la proteína se adsorbe a una fase estacionaria.
¿Cómo se puede mejorar el rendimiento de la renaturación?
Se pueden utilizar diversos aditivos en el búfer de renaturación para mejorar la solubilidad y minimizar las reacciones secundarias, como la agregación. Estos aditivos incluyen chaperonas moleculares (que asisten el plegamiento), agentes caotrópicos a baja concentración, sales, azúcares, y detergentes suaves. Además, la optimización de la velocidad de eliminación del desnaturalizante, la concentración de proteína inicial y la temperatura son cruciales.
¿Cuáles son los 7 tipos principales de proteínas?
Las proteínas son extremadamente diversas en función y estructura. Se pueden clasificar en siete tipos principales según su rol biológico:
- Anticuerpos: Proteínas del sistema inmune que identifican y neutralizan patógenos.
- Proteínas contráctiles: Involucradas en el movimiento, como la actina y la miosina en los músculos.
- Enzimas: Catalizan reacciones bioquímicas, acelerando procesos vitales (ej., amilasa, pepsina).
- Proteínas hormonales: Señalizan y regulan procesos biológicos a distancia (ej., insulina, hormona del crecimiento).
- Proteínas estructurales: Proporcionan soporte y forma a células y tejidos (ej., colágeno, queratina).
- Proteínas de almacenamiento: Almacenan iones metálicos y aminoácidos (ej., ferritina para hierro, caseína para nutrientes).
- Proteínas de transporte: Mueven moléculas esenciales a través de membranas o por el cuerpo (ej., hemoglobina para oxígeno, canales de iones).
La renaturación de estas diversas proteínas es un campo en constante evolución, crucial para la biotecnología y la comprensión fundamental de cómo las proteínas adquieren su forma y función. Con una variedad de enfoques y la posibilidad de combinarlos, los científicos continúan mejorando los rendimientos y la eficiencia de este complejo pero vital proceso.
Si quieres conocer otros artículos parecidos a Renaturación de Proteínas: Desentrañando el Proceso puedes visitar la categoría Nacionalidad.

