19/09/2018
Las proteínas son, sin lugar a dudas, los 'caballos de batalla' de nuestras células. Estas macromoléculas complejas desempeñan una infinidad de roles cruciales en los organismos vivos, desde proporcionar estabilidad estructural y actuar como motores de movimiento, hasta llevar a cabo actividades metabólicas, participar en la expresión de información genética y mediar la comunicación celular. Aunque se sintetizan en diversas formas y tamaños, todas comparten un bloque de construcción común: los aminoácidos. Comprender la intrincada naturaleza de las proteínas es fundamental para desentrañar los misterios de la vida. Este artículo se adentrará en sus niveles estructurales, explorará el fenómeno de la desnaturalización y su sorprendente reversibilidad (renaturalización), y destacará la vital propiedad de la especificidad.
- Las Cuatro Estructuras Fundamentales de las Proteínas
- Desnaturalización Proteica: ¿Qué es y Por Qué Ocurre?
- Renaturalización: El Regreso a la Forma Original
- La Fascinante Especificidad de las Proteínas
- Preguntas Frecuentes sobre Proteínas y su Estructura
- ¿Por qué es tan importante la estructura primaria para la función de una proteína?
- ¿Qué sucede si una proteína se desnaturaliza y no puede renaturalizarse?
- ¿Todas las proteínas tienen los cuatro niveles de estructura?
- ¿Cómo ayudan las chaperonas en el plegamiento de proteínas?
- ¿Qué implicaciones tiene la especificidad de las proteínas en la salud humana?
Las Cuatro Estructuras Fundamentales de las Proteínas
La funcionalidad de una proteína está intrínsecamente ligada a su forma tridimensional, la cual se organiza en cuatro niveles jerárquicos. Cada nivel contribuye a la configuración global y, por ende, a la función biológica de la proteína.
Estructura Primaria: La Secuencia de la Vida
La estructura primaria de una proteína se define por la secuencia única y lineal de sus aminoácidos. Esta secuencia es la base fundamental de su función. Imaginemos una proteína como una cadena de cuentas, donde cada cuenta representa un aminoácido específico. El orden en que estas cuentas están enhebradas es crucial. Por ejemplo, una simple mutación en la hemoglobina, que reemplaza un ácido glutámico por valina en la posición 6 de la cadena β-globina, resulta en la anemia de células falciformes. Este cambio aparentemente minúsculo en la secuencia primaria tiene consecuencias devastadoras para la función de la proteína y la salud del individuo. La estructura primaria es, por tanto, el código genético expresado, el plan maestro que determina los niveles superiores de organización proteica.
Estructura Secundaria: Los Primeros Plegamientos
La estructura secundaria se forma a través de interacciones entre los grupos funcionales del esqueleto peptídico, excluyendo los grupos R o cadenas laterales de los aminoácidos. Estas estructuras se distinguen por segmentos con formas específicas, estabilizadas principalmente por puentes de hidrógeno. Estos enlaces se forman entre el oxígeno del grupo carbonilo (C=O) de un residuo de aminoácido y el hidrógeno del grupo amino (N-H) de otro aminoácido. Los dos tipos más comunes de estructura secundaria son:
- Hélice alfa (α-hélice): En esta conformación, el esqueleto polipeptídico se enrolla en una espiral helicoidal. Los puentes de hidrógeno se forman entre residuos que están separados por solo cuatro posiciones lineales en la secuencia.
- Hoja beta plegada (β-plegada): Aquí, segmentos de la cadena peptídica se doblan 180° y luego se pliegan en el mismo plano, formando una estructura similar a un acordeón. La distancia entre los residuos que forman puentes de hidrógeno puede ser mayor, ya que los pliegues de la cadena los acercan en el espacio tridimensional.
La secuencia primaria de una proteína influye directamente en la formación de estas estructuras secundarias. Algunos aminoácidos son más propensos a formar α-hélices, mientras que otros favorecen las β-plegadas. Por ejemplo, la prolina, debido a su inusual grupo R, rara vez se encuentra en α-hélices.
Estructura Terciaria: La Forma Tridimensional Completa
La estructura terciaria es la configuración tridimensional completa y distintiva de una proteína, incluyendo todos sus átomos del esqueleto y todas sus cadenas laterales. Surge de las interacciones entre los grupos R de los aminoácidos a medida que la cadena se dobla y pliega en el espacio tridimensional. A diferencia de las estructuras secundarias, que involucran principalmente puentes de hidrógeno en el esqueleto, las estructuras terciarias son el resultado de una diversidad de enlaces e interacciones entre los grupos R o entre los grupos R y el esqueleto. Estas interacciones pueden ocurrir entre residuos que están muy distantes en la secuencia lineal.
Los tipos clave de interacciones químicas involucradas incluyen:
- Puentes de hidrógeno: Entre cadenas laterales polares o entre cadenas laterales y el esqueleto.
- Interacciones hidrofóbicas: En una solución acuosa, las cadenas laterales no polares tienden a agruparse en el núcleo de la proteína, lejos del agua, formando masas globulares.
- Interacciones de van der Waals: Una vez que las cadenas laterales hidrofóbicas están cerca, su asociación se estabiliza aún más por estas atracciones eléctricas débiles.
- Puentes disulfuro: Enlaces covalentes fuertes que se forman entre los grupos sulfhidrilo de dos cisteínas. Actúan como 'puentes' que conectan regiones distintas de la misma cadena polipeptídica o de dos polipéptidos separados.
- Enlaces iónicos: Se forman entre grupos con cargas opuestas, como los grupos R ácidos y básicos ionizados.
A medida que un polipéptido se pliega en su forma correcta, los aminoácidos con cadenas laterales no polares suelen agruparse en el núcleo de la proteína, evitando el contacto con el agua. Aunque individualmente débiles, el efecto acumulativo de estas interacciones es crucial para determinar la forma distintiva de la proteína. La estructura primaria desempeña un papel fundamental en la determinación de la estructura terciaria y la función global de la proteína.
Estructura Cuaternaria: La Unión de Subunidades
Mientras que las estructuras primaria, secundaria y terciaria involucran polipéptidos individuales, algunas proteínas son más complejas y contienen múltiples cadenas polipeptídicas que interactúan para formar una única estructura funcional. Estas combinaciones de polipéptidos, denominadas subunidades, otorgan a estas proteínas una estructura cuaternaria. La disposición espacial de todas las cadenas es esencial para mantener la función y estabilidad de las proteínas multicatenarias. Las subunidades individuales se mantienen unidas por los mismos tipos de enlaces e interacciones que se encuentran en el nivel terciario de la estructura (puentes de hidrógeno, interacciones hidrofóbicas, van der Waals, puentes disulfuro y enlaces iónicos).
A continuación, una tabla comparativa para visualizar las diferencias entre las estructuras:
| Estructura | Descripción | Interacciones Clave | Ejemplos/Características |
|---|---|---|---|
| Primaria | Secuencia lineal de aminoácidos. | Enlaces peptídicos (covalentes). | Determina todos los niveles superiores. Un cambio altera la función. |
| Secundaria | Plegamientos locales del esqueleto polipeptídico (α-hélice, β-plegada). | Puentes de hidrógeno entre átomos del esqueleto. | Formas regulares y repetitivas. |
| Terciaria | Forma tridimensional completa de una sola cadena polipeptídica. | Puentes de hidrógeno, interacciones hidrofóbicas, van der Waals, puentes disulfuro, enlaces iónicos (entre grupos R). | Define la función biológica específica. |
| Cuaternaria | Disposición espacial de múltiples subunidades polipeptídicas. | Mismas interacciones que la terciaria (entre subunidades). | Solo en proteínas con más de una cadena polipeptídica. |
Desnaturalización Proteica: ¿Qué es y Por Qué Ocurre?
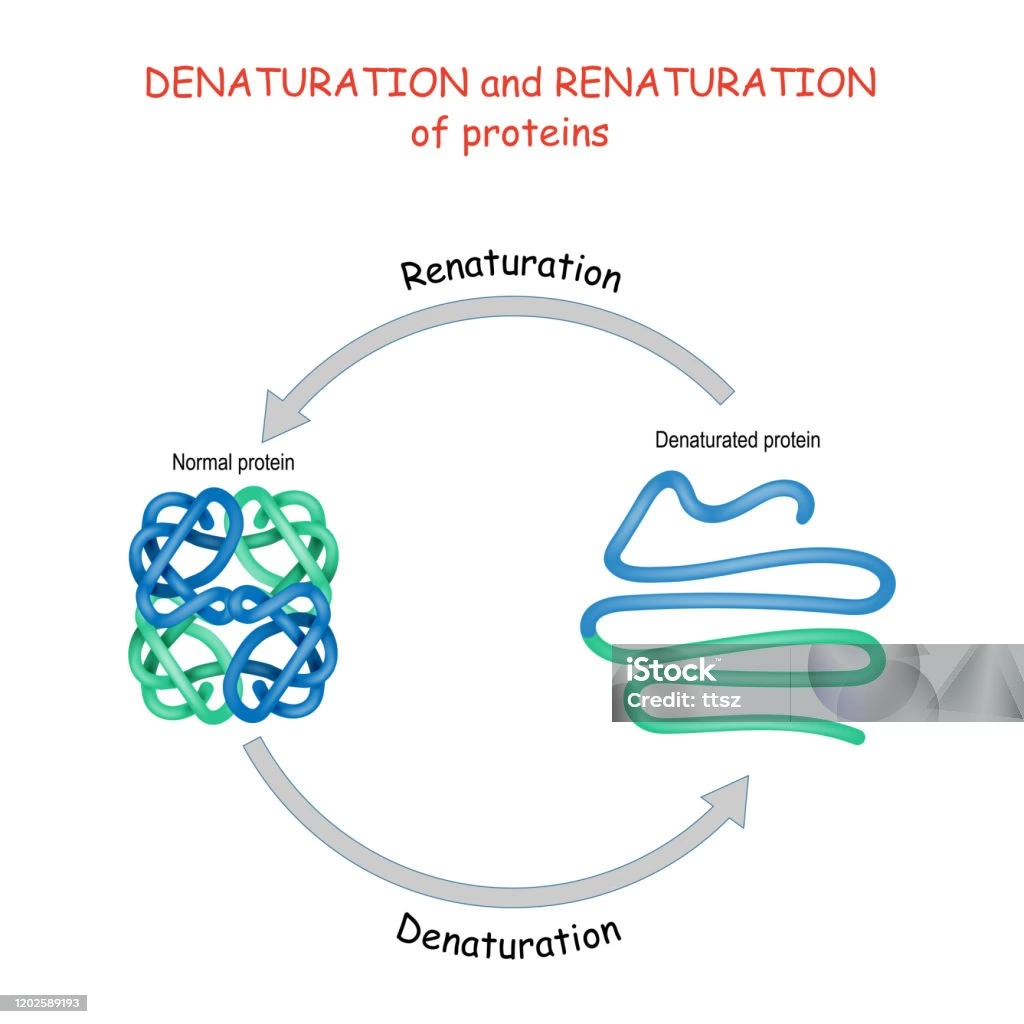
La desnaturalización es un proceso crítico en la biología de las proteínas que implica la pérdida de sus estructuras cuaternaria, terciaria y secundaria, conservándose únicamente la estructura primaria. Cuando una proteína se desnaturaliza, se transforma en filamentos lineales y delgados que pueden entrelazarse, formando compuestos fibrosos e insolubles en agua. Este fenómeno es el motivo por el cual un huevo cocido cambia de líquido transparente a sólido blanco: las proteínas de la clara se desnaturalizan y coagulan.
Los agentes que pueden causar la desnaturalización de una proteína son variados y pueden incluir:
- Calor excesivo: La mayoría de las proteínas experimentan desnaturalización cuando se calientan entre 50 y 60 °C. Las altas temperaturas aumentan la energía cinética de las moléculas, rompiendo los enlaces débiles que mantienen la estructura tridimensional.
- Sustancias que modifican el pH: Cambios extremos en el pH (muy ácidos o muy básicos) alteran el estado de ionización de los grupos R de los aminoácidos, afectando los enlaces iónicos y los puentes de hidrógeno.
- Alteraciones en la concentración: Cambios en la concentración de sales o solventes pueden afectar las interacciones hidrofóbicas y la capa de solvatación alrededor de la proteína.
- Alta salinidad: Una concentración excesiva de sales puede competir con las proteínas por las moléculas de agua, interrumpiendo las interacciones hidrofóbicas y los puentes de hidrógeno.
- Agitación molecular: La agitación vigorosa puede romper los delicados enlaces que mantienen la estructura tridimensional.
- Solventes orgánicos o detergentes: Estos pueden interferir con las interacciones hidrofóbicas, causando el desplegamiento de la proteína.
El efecto más visible de este fenómeno es que las proteínas se vuelven menos solubles o completamente insolubles, y lo más importante, pierden su actividad biológica. Una enzima desnaturalizada, por ejemplo, ya no puede catalizar su reacción específica. Es crucial entender que la desnaturalización no rompe los enlaces peptídicos que forman la estructura primaria; solo afecta los niveles superiores de organización.
Renaturalización: El Regreso a la Forma Original
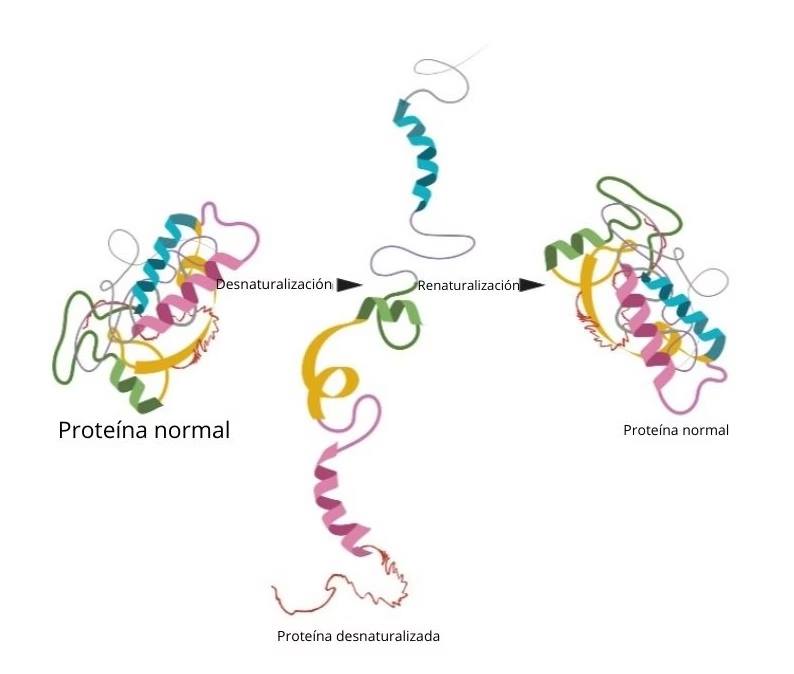
Aunque la desnaturalización a menudo se percibe como un proceso irreversible, estudios científicos han demostrado convincentemente que la desnaturalización de proteínas puede ser un proceso reversible, conocido como renaturalización. Esto significa que las proteínas que han sido desnaturalizadas por agentes como el calor, pH extremos o ciertos reactivos desnaturalizantes, pueden recuperar su estructura nativa (original) y su función biológica si se les regresa a condiciones que favorecen esa conformación.
Un ejemplo clásico de renaturalización ocurre con la ribonuclease. Esta enzima puede ser desnaturalizada en presencia de urea y mercaptoetanol, un agente reductor que rompe los puentes disulfuro. Sin embargo, al eliminar la urea y el mercaptoetanol del medio, la ribonuclease es capaz de recuperar espontáneamente su conformación nativa y, con ella, su actividad enzimática. Este experimento es una prueba contundente de que la información necesaria para el plegamiento correcto de una proteína reside íntegramente en su estructura primaria.
El proceso de renaturalización subraya la importancia crítica de la secuencia de aminoácidos. Es esta secuencia la que dicta cómo se plegará la proteína en su forma tridimensional funcional. Aunque muchas proteínas pueden pasar por varias estructuras intermedias antes de alcanzar su conformación más estable, estas intermedias no son visibles en la proteína plegada final.
En el entorno celular, existen moléculas especializadas llamadas chaperonas o chaperoninas, que son proteínas que asisten en el plegamiento correcto de otras proteínas. Estas moléculas desempeñan un papel crucial al proteger a los polipéptidos recién sintetizados de condiciones químicas disruptivas en el citoplasma y al permitir que se plieguen espontáneamente de manera eficiente. Los defectos en el plegamiento de proteínas son la base molecular de varias enfermedades genéticas, lo que resalta la importancia de la renaturalización y el correcto plegamiento para la salud celular.

La Fascinante Especificidad de las Proteínas
Una de las propiedades más notables y características de las proteínas es su especificidad. A diferencia de los glúcidos y lípidos, que son comunes a todas las formas de vida, cada especie de ser vivo es capaz de fabricar sus propias proteínas, que difieren de las de otras especies. Incluso dentro de una misma especie, existen diferencias proteicas entre los distintos individuos. Esta enorme diversidad proteica, tanto interespecífica como intraespecífica, es una consecuencia directa de las múltiples combinaciones posibles entre los aminoácidos, una combinación que está determinada por el ADN único de cada individuo.
La especificidad de las proteínas explica fenómenos biológicos cruciales como la compatibilidad o incompatibilidad en los trasplantes de órganos, los injertos biológicos, el uso de sueros sanguíneos, los procesos alérgicos e incluso la susceptibilidad a ciertas infecciones. En esencia, la forma y la composición química de una proteína le permiten interactuar de manera precisa con otras moléculas.
Especificidad Enzimática: Precisión Molecular
La especificidad es particularmente evidente en el ámbito de las enzimas. La especificidad de una enzima se refiere a la capacidad de una enzima particular para interactuar con su sustrato correspondiente. Las interacciones entre una proteína (como una enzima) y su ligando (como un sustrato) afectan sustancialmente la especificidad. Se sabe que las interacciones electrostáticas y las interacciones hidrofóbicas son las más influyentes en la determinación de esta especificidad. La fuerza de estas interacciones se correlaciona positivamente con la especificidad entre la enzima y el sustrato.
Las enzimas varían en la especificidad de los sustratos a los que se unen para llevar a cabo funciones fisiológicas específicas. Algunas enzimas pueden ser menos específicas, uniéndose a numerosos sustratos para catalizar una reacción. Otras, sin embargo, requieren una especificidad extrema para un único sustrato para que se produzca una reacción adecuada y un fenotipo fisiológico. Los diferentes tipos de especificidad enzimática se dividen generalmente en cuatro grupos:
- Especificidad absoluta: Una enzima actúa sobre un único sustrato específico. Por ejemplo, la lactasa solo degrada la lactosa, y la glucoquinasa fosforila exclusivamente la glucosa.
- Especificidad de grupo: La enzima reacciona solo con moléculas que poseen grupos funcionales específicos (como estructuras aromáticas, grupos fosfato o metilos). La pepsina, por ejemplo, hidroliza los enlaces peptídicos entre aminoácidos hidrofóbicos con cadenas laterales aromáticas. La hexoquinasa, por su parte, fosforila múltiples hexosas (azúcares de seis carbonos).
- Especificidad de enlace: La enzima reconoce y escinde tipos particulares de enlaces químicos, independientemente de los grupos funcionales específicos.
- Especificidad estereoquímica: Este tipo de especificidad es sensible a la orientación espacial (actividad óptica) del sustrato. Por ejemplo, la beta-glucosidasa solo reacciona con enlaces beta-glucosídicos, como los presentes en la celulosa, pero no con los alfa-glucosídicos del almidón.
Determinación y Significado de la Especificidad
La especificidad química de una enzima para un sustrato particular se puede cuantificar utilizando variables derivadas de la ecuación de Michaelis-Menten, como la constante de disociación de equilibrio (Kd) o la relación kcat/Km, conocida como la constante de especificidad. Esta constante proporciona una medida de la afinidad de un sustrato por una enzima particular y es un indicador de la eficiencia de la enzima; cuanto mayor es la constante de especificidad, mayor es la preferencia de la enzima por ese sustrato.
La relevancia de la especificidad proteica se extiende a la investigación médica y al descubrimiento de fármacos. Comprender la especificidad enzimática proporciona información valiosa sobre la estructura de la enzima y sus funciones fisiológicas. En el desarrollo de nuevos medicamentos, es fundamental que estos contengan estructuras lo más específicas posible para su molécula objetivo, minimizando así los efectos fuera del objetivo que podrían producir síntomas desfavorables en el paciente. Los medicamentos dependen de la especificidad de las moléculas diseñadas para inhibir dianas moleculares particulares.
Aplicaciones de la Especificidad Proteica
Varias técnicas científicas se basan en la especificidad química de las proteínas, especialmente la de los anticuerpos. Por ejemplo:
- Inmunotinción: Utiliza la especificidad de los anticuerpos para detectar una proteína de interés a nivel celular, permitiendo a los investigadores visualizar su ubicación dentro de las células o tejidos.
- Transferencia Western (Western blot): Esta técnica se emplea para detectar una proteína específica de interés en una muestra de tejido. Implica la separación de proteínas por electroforesis en gel, seguida de la transferencia a una membrana que luego se incuba con anticuerpos. Estos anticuerpos son específicos de la proteína objetivo y a menudo llevan una etiqueta fluorescente o enzimática que indica la presencia de la proteína.
Estas aplicaciones demuestran la importancia fundamental de la especificidad proteica no solo en la función biológica, sino también como una herramienta indispensable en la investigación y el diagnóstico médico.

Preguntas Frecuentes sobre Proteínas y su Estructura
¿Por qué es tan importante la estructura primaria para la función de una proteína?
La estructura primaria, que es la secuencia lineal de aminoácidos, es fundamental porque determina cómo la proteína se plegará en sus estructuras secundaria, terciaria y, si aplica, cuaternaria. Cualquier cambio en esta secuencia (como una mutación genética) puede alterar la forma tridimensional de la proteína y, por lo tanto, su capacidad para realizar su función biológica. Es el plano de construcción que dicta la forma final y la función.
¿Qué sucede si una proteína se desnaturaliza y no puede renaturalizarse?
Si una proteína se desnaturaliza irreversiblemente, pierde permanentemente su forma tridimensional funcional. Esto significa que ya no puede llevar a cabo su papel biológico. Por ejemplo, una enzima desnaturalizada no puede catalizar reacciones, y una proteína estructural desnaturalizada no puede mantener la integridad de una célula. En muchos casos, las proteínas desnaturalizadas se agregan y precipitan, volviéndose insolubles.
¿Todas las proteínas tienen los cuatro niveles de estructura?
No, no todas las proteínas tienen los cuatro niveles de estructura. Todas las proteínas tienen estructura primaria, secundaria y terciaria. Sin embargo, la estructura cuaternaria solo existe en proteínas que están compuestas por dos o más cadenas polipeptídicas (subunidades) que interactúan entre sí para formar una única unidad funcional. Un ejemplo es la hemoglobina, que tiene cuatro subunidades.
¿Cómo ayudan las chaperonas en el plegamiento de proteínas?
Las chaperonas son proteínas especializadas que asisten en el plegamiento correcto de otras proteínas. Actúan creando un ambiente protegido donde los polipéptidos pueden plegarse sin interferencias de otras moléculas o condiciones adversas del citoplasma. No dictan el plegamiento, sino que facilitan que el polipéptido alcance su conformación nativa de manera espontánea, basándose en la información contenida en su estructura primaria.
¿Qué implicaciones tiene la especificidad de las proteínas en la salud humana?
La especificidad de las proteínas tiene enormes implicaciones en la salud humana. Es la base de la compatibilidad en trasplantes de órganos (compatibilidad de proteínas de superficie celular), la respuesta inmune (anticuerpos específicos para patógenos), el funcionamiento de los medicamentos (diseñados para unirse específicamente a dianas moleculares) y la comprensión de enfermedades genéticas (causadas por proteínas con especificidad alterada). Sin esta propiedad, muchos procesos biológicos esenciales no podrían ocurrir de manera precisa y eficiente.
En conclusión, el mundo de las proteínas es un testimonio de la precisión y complejidad de la vida. Desde la simple secuencia de aminoácidos en su estructura primaria hasta las intrincadas interacciones que definen su forma tridimensional y su capacidad de renaturalización, cada aspecto de las proteínas es crucial para su función. Su asombrosa especificidad les permite actuar como los actores precisos y versátiles que mantienen en funcionamiento todos los procesos vitales de los organismos. Comprender estos principios no solo enriquece nuestro conocimiento biológico, sino que también abre puertas a avances significativos en medicina y biotecnología.
Si quieres conocer otros artículos parecidos a El Fascinante Mundo de las Proteínas: Estructura y Función puedes visitar la categoría Nacionalidad.
